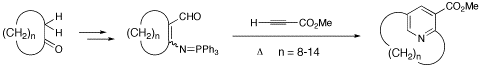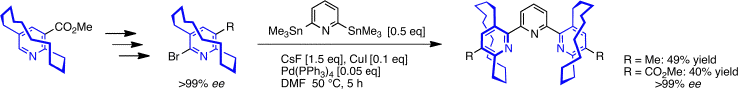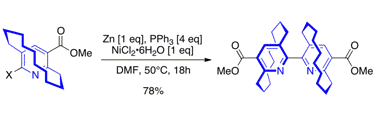| 研究概要 |
| 本研究室では「新規機能性有機分子の設計、合成、および反応性に関する研究」を総括研究課題とし,有機化学的手法を用いて主に構造有機化学・複素環化学・生物有機化学の観点から研究を行っている。面性キラリティーを持つシクロファン分子や補酵素NAD類似機能を持つ生体モデル分子,天然物類似の生物活性機能を有する天然物アナローグなど,様々な機能性分子の合成と機能探索を研究対象としている。具体的には, (1)構造由来の独自機能を活かした分子設計 (2)機能性複素環分子の新合成法の開発 (3)非天然型有機触媒と新規有用反応の探索 (4)動的不斉変換法の開発 (5)天然型および非天然型の生物活性化合物の合成と機能に関する研究 を主な研究課題に定めて研究を進めている。特に分子構造と機能性発現機構の関係に着目し,分光学的手法,結晶解析,計算化学的手法を用いた構造解析と,不斉有機合成,生物活性機能への応用を指向している。 |
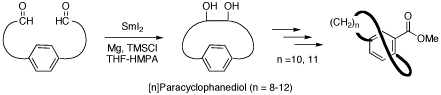
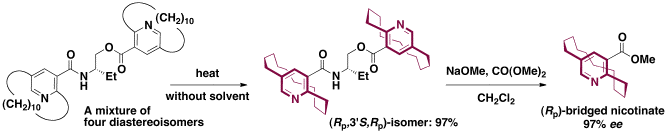
面不斉シクロファン,ピリジノファンの新規合成法開発とその応用
Kanomata, N.; Yamada, S.; Ohhama, T.; Fusano, A.; Ochiai, Y.; Oikawa, J.; Yamaguchi, M.; Sudo, F. "Synthesis of Bridged Nicotinates Having [n](2,5)Pyridinophane Skeletons (n = 8-14),"Tetrahedron 2006, 62, 4128-4138.
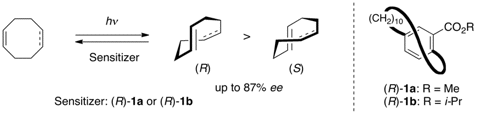
Maeda, R.; Wada, T.; Mori, S.; Kono, S.; Kanomata, N.; Inoue, Y. "Planar-to-Planar Chirality Transfer in the Excited State. Enantiodif-ferentiating Photoisomerization of Cyclooctenes Sensitized by Planar-Chiral Paracyclophane," J. Am. Chem. Soc. 2011, 133, 10379-10381.
|
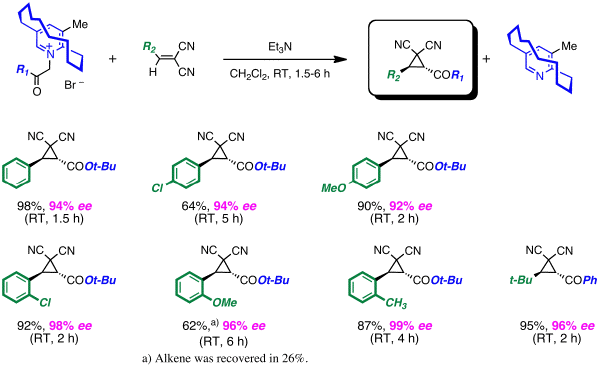
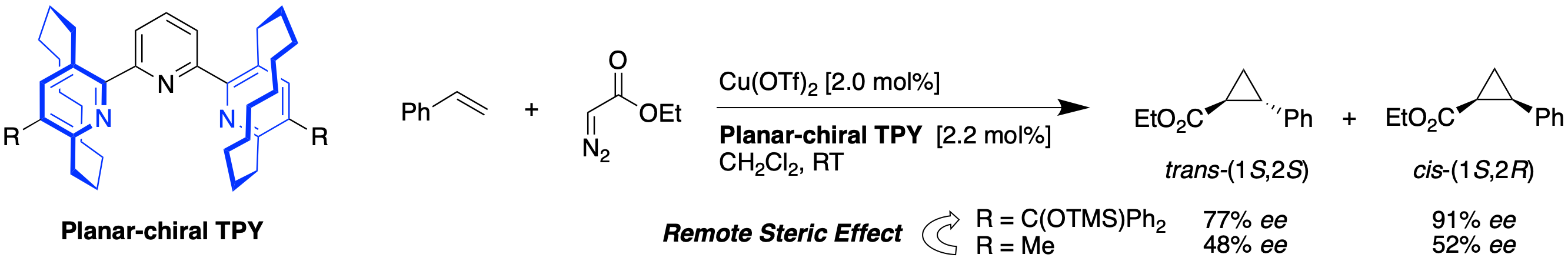
面不斉ピリジニウムイリドによる不斉シクロプロパン化反応
|
面不斉ピリジンリガンドの合成と不斉触媒への応用
Kanomata, N.; Suzuki, J.; Kubota, H.; Nishimura, K.; Enomoto, T. "Synthesis of planar-chiral bridged bipyridines and terpyridines by metal-mediated coupling reactions of pyridinophanes," Tetrahedron Lett. 2009, 50, 2740-2743.
|
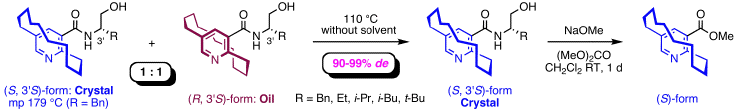
シクロファン誘導体を用いた面性キラリティーの熱的制御に関する研究
|
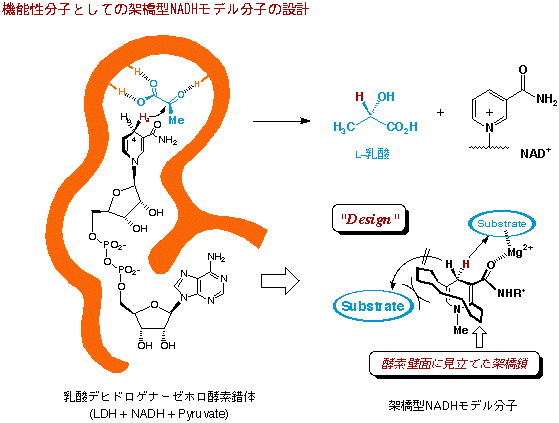
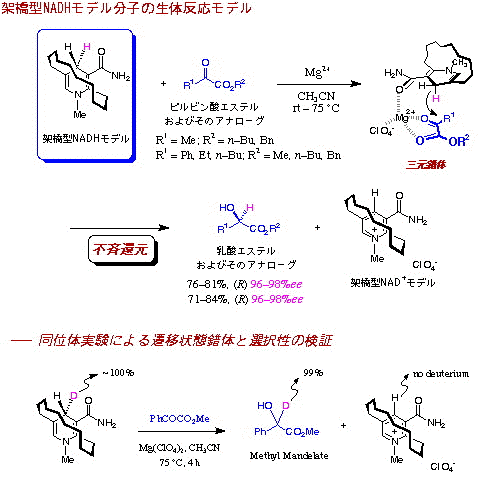
触媒機能を指向した酸化還元型補酵素モデル反応の開発研究
Kanomata, N.; Nakata, T. "Highly Enantioselective Reduction with Novel, Bridged NADH Models," Angew. Chem. Int. Ed. Engl. 1997, 36, 1207-1211.
Kanomata, N.; Nakata, T. "A Compact Chemical Miniature of a Holoenzyme, Coenzyme NADH Linked Dehydrogenase. Design and Synthesis of Bridged NADH Models and Their Highly Enantioselective Reduction," J. Am. Chem. Soc. 2000, 122, 4563-4568.
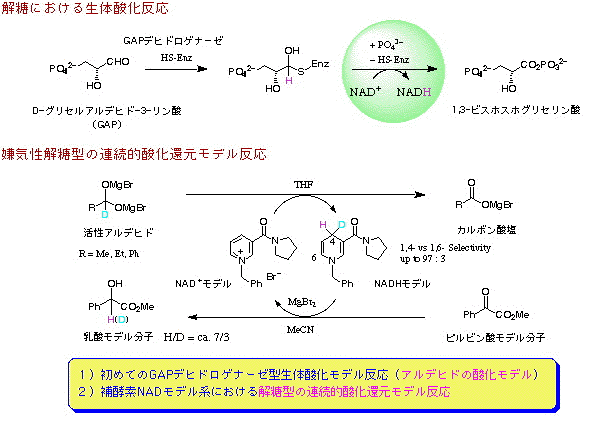
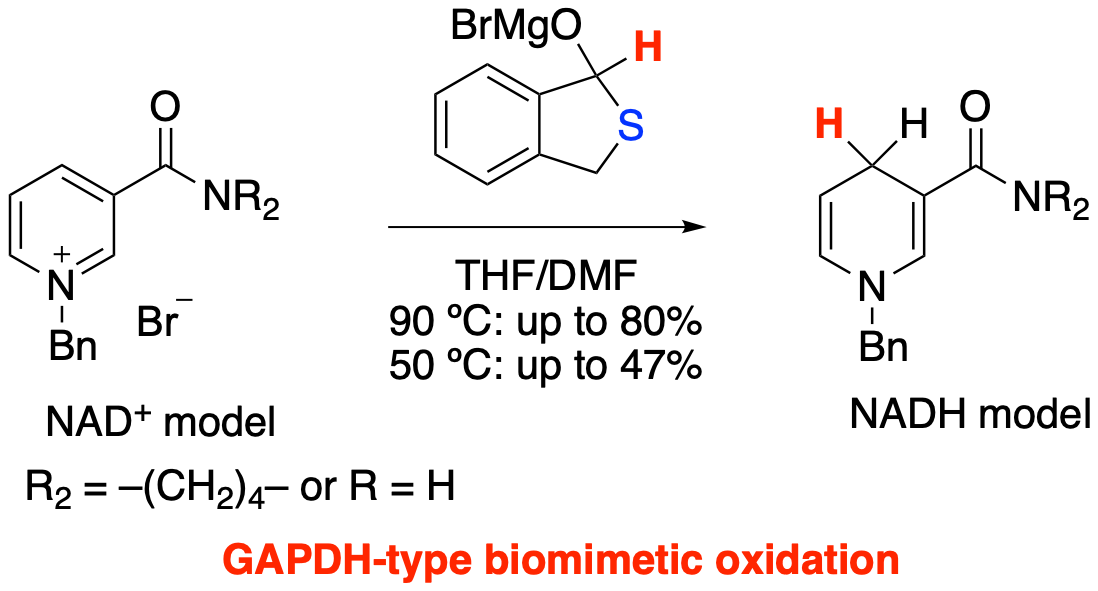
Kanomata, N.; Yohida, M.; Suzuki, M.; Nakata, T. "Biomimetic Oxidation of Aldehyde with NAD + Models: Glycolysis-Type Hydrogen Transfer in an NAD+/NADH Model System," Angew. Chem. Int. Ed. 1998, 37, 1410-1412. GAPDHのシステイン残基由来のモデル基質を用いて反応を行った場合,完全な位置選択性かつ高収率でNADHモデルを与えることを見いだした.この結果は,硫黄原子の代わりに酸素原子をもつ非天然型のセリン残基由来のモデル基質を用いた場合はNADHモデル分子が僅かにしか生成しないことと好対照である.本研究の結果は,GADPH酵素内における基質の活性化にシステイン残基が選択されていることの妥当性を実験的に明らかにした初めての知見であり,硫黄の高い電子供与効果がその要因として考えられることが示された. Ogawa, N.; Furukawa, S.; Kosugi, Y.; Takazawa, T.; Kanomata, N. "Biomimetic systems involving sequential redox reactions in glycolysis -the sulfur effect," Chem. Commun. 2020, 56, 12917-12920. 天然型および非天然型生物活性化合物の合成とその機能性研究
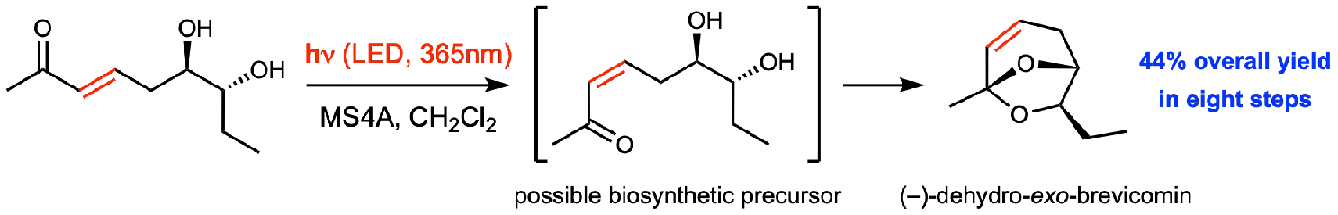
Hirasawa, S.; Masuda, T.; Mukai, K.; Miyoshi, Y.; Kanomata, N. "Asymmetric synthesis of (−)-dehydro-exo-brevicomin with a photoisomerisation-intramolecular acetalisation sequence," Org. Biomol. Chem. 2021, 19, 6897-6903.
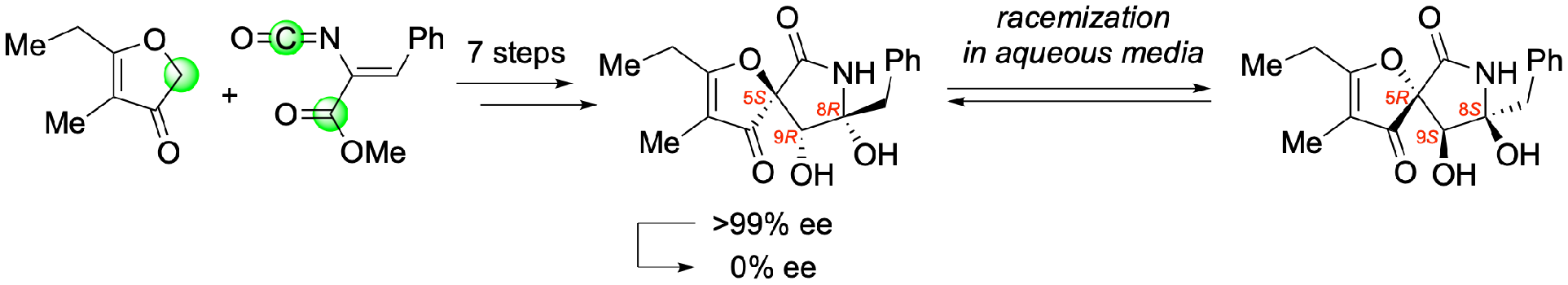
Hirasawa, S.; Mukai, K.; Sakai, S.; Wakamori, S.; Hasegawa, T.; Souma, K.; Kanomata, N.; Ogawa, N.; Aizawa, M.; Emoto, M. "Elucidation of Racemization Process of Azaspirene Skeleton in Neutral Aqueous Media," J Org Chem. 2018, 83, 14457-14464.
|