トリインの触媒的不斉[2+2+2]付加環化反応
[2+2+2]付加環化反応、すなわちアルキンの三量化反応は、置換ベンゼン環誘導体を与える最も原子効率が高い反応である。
末端にオルト置換アリール基をもつジインとアルキンとの反応においてキラルなイリジウム触媒を用いると、 付加環化反応が高エナンチオ、かつジアステレオ選択的に進行し、 2つの軸不斉をもつC2対称なポリアリール化合物を与えた。
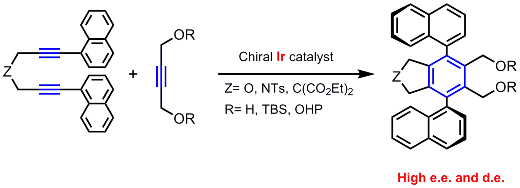
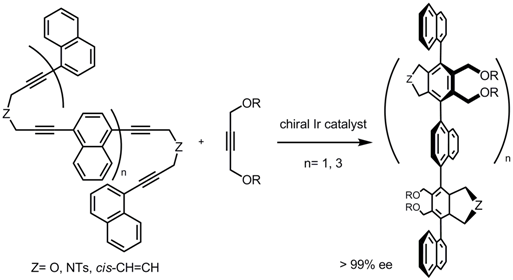
本反応の高立体選択性を活かして、ジイン部位を複数有するポリインを基質として用いるキラルポリアリール化合物の合成を試みた。 テトライン(n=1)およびオクタイン(n=3)からポリアリール化合物がほぼ完全なエナンチオかつジアステレオ選択的に得られた。
これは、キラルイリジウム触媒が4つもしくは8つもの連続した軸不斉を完全に制御したことを意味する。
テトラフェニレン誘導体への応用
テトラフェニレンとは、4つのベンゼンが全てオルト位で連結した環状化合物である。 中心部分のオクタテトラエン骨格は、剛直な鞍型構造であり、ベンゼン環上への置換基の導入によりキラル化合物となり、 新規な光学活性π電子共役系化合物として期待されている。
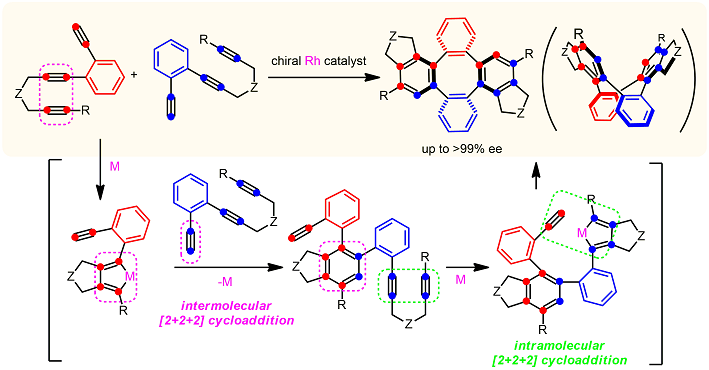
我々は、ベンゼン環のオルト位にエチニル基と1,6-ジイン部分を有するトリインを基質として用い、キラルロジウム触媒存在下反応させた。 その結果、最初に分子間で1,6-ジイン部分とエチニル基が反応し、引き続き分子内で未反応のエチニル基と1,6-ジインが反応することにより、 連続的 [2+2+2]付加環化反応が進行し、キラルな置換テトラフェニレン化合物が高不斉収率で得られた。
本法は、新規かつ簡便なテトラフェニレン骨格構築法であるのみならず、初めての高エナンチオ選択的な合成例である。
参考文献
- Shibata, T.; Fujimoto, T.; Yokota, K.; Takagi, K. J. Am. Chem. Soc. 2004, 126, 8382–8383.
- Shibata, T.; Arai, Y.; Takami, K.; Tsuchikama, K.; Fujimoto, T.; Takebayashi, S.; Takagi, K. Adv. Synth. Catal. 2006, 348, 2475–2483.
-
Shibata, T.; Tsuchikama, K.
Chem. Commun. 2005, 6017–6019.
Highlighted in Synfacts 2006, 230. -
Shibata, T.; Chiba, T.; Hirashima, H.; Ueno, Y.; Endo, K.
Angew. Chem. Int. Ed. 2009, 48, 8066–8069.
Chosen as VIP & Highlighted in Angew. Chem. Int. Ed. 2010, 49, 672–674.
総合論文
- 柴田 高範, 有機合成化学協会誌 2006, 64, 913–922.
- Shibata, T.; Tsuchikama, K. Org. Biomol. Chem. 2008, 1317–1323.
- 柴田 高範; 土釜 恭直, ファインケミカル (2008年5月号), 55–67.