研究内容
1.フラビン誘導体を用いる不斉バイヤービリガー反応
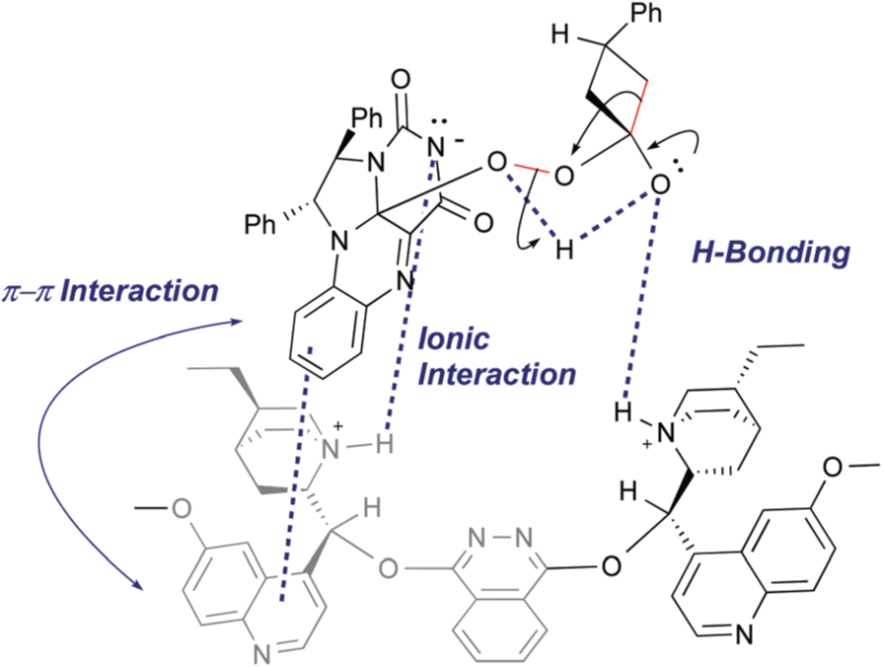
環境負荷が低く効率性の高い触媒の開発は、持続可能な開発目標(SDGs)を実現させる上で大切な目標の一つとなっています。 一方、生体内の反応をつかさどる酵素反応は、高い反応性・選択性に加えて環境負荷ゼロであり、触媒の完全型ともいえますが、反応条件や基質適用範囲などの実際の使用には難しい面もあります。 そこで、当研究室では酵素反応を触媒する鍵分子となる補酵素、特に一般的な補酵素の一つであるフラビンの誘導体を用いた反応の開発に取り組んでいます。 特に、フラビンの誘導体と光学活性な天然物であるシンコナアルカロイドを溶液中で自己集合させることで、フラビン誘導体により促進される酸化反応の一つであるバイヤービリガー反応が高い立体選択性で進むことを見出しました。 これは、フラビン誘導体に弱い結合で不斉因子を付加することで、立体選択性を得た最初の例となります。 最近では、反応の律速段階や不斉に関わる要因の特定を行い、基質適用範囲の拡張させ立体選択性を最高99%e.e.まであげることに成功しました。
2.動的速度論光学分割を伴う不斉リン原子酸素化反応
リンの3つの置換基がすべて異なる化合物は、リンが不斉中心となるため、P-キラル化合物といいます。これらの化合物は、金属触媒のリガンド、有機触媒、あるいは市販薬の原薬などとして幅広く用いられています。 このような化合物の合成には効率の良い触媒反応が数少なく、それも汎用性の高いものはありません。そこで、当研究室ではフラビン誘導体はヘテロ原子の酸化を得意としていることから 発想を得て、リンの酸化も触媒することを見出しました。現在、この反応をさらに不斉酸化反応に発展させることを目指して研究を続けています。
3.リン不斉修飾核酸の立体選択的合成法の開発
核酸医薬品はコロナのワクチンにも適用されたことからも分かるように、これからの発展が期待できる分野です。天然型の核酸は不安定であるため、核酸医薬品には様々な部位を変えた修飾核酸が用いられています。 このような修飾核酸で主要なものは、リン酸部位の水酸基をほかの官能基に変換したP-キラルなリン酸骨格を持つものです。このリンの立体化学は生理活性に大きく影響するため、高い純度で合成することが重要です。 当研究室では、特にリン不斉中心を触媒的に構築すること、核酸伸長に要する段階数を短段階に抑えること、の2点にこだわったリン不斉修飾核酸の不斉合成法の開発に取り組んでいます。
4.天然物合成
2022年から生理活性のある天然物をターゲットにした天然物合成研究も始めました。共同研究により生理活性の作用機序を見出すことも目標としています。
論文
1.Structure–selectivity correlation in asymmetric Baeyer–Villiger oxidation of 3-arylcyclobutanones by a flavinium ion-pair catalyst



